2026 Автор: Howard Calhoun | calhoun@techconfronts.com. Акыркы өзгөртүү: 2025-06-01 07:14:29
Электрдик диссоциация жашообузда чоң роль ойнойт, бирок биз бул жөнүндө көбүнчө ойлонбойбуз. Дал ушул кубулуш менен суюк чөйрөдөгү туздардын, кислоталардын жана негиздердин электр өткөргүчтүгү байланышкан. Сексен пайыз суюктук болгон адамдын денесиндеги «тирүү» электр кубаты пайда болгон алгачкы жүрөктүн кагышынан баштап, батарейкалары негизинен электрохимиялык батарейкалар болгон унааларга, уюлдук телефондорго жана оюнчуларга чейин, электрдик диссоциация көзгө көрүнбөй жаныбызда бар.
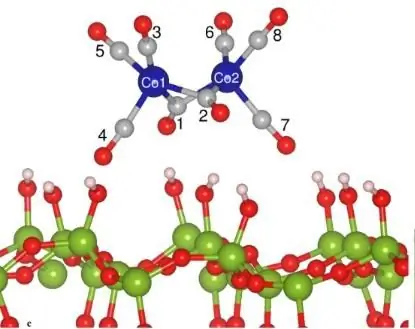
Жогорку температурада эриген бокситтен уулуу түтүн чыгарган гиганттык идиштерде электролиз жолу менен "канаттуу" металл - алюминий алынат. Айланабыздагы бардык нерсе, хром радиатордук торлордон баштап кулагыбыздагы күмүш жалатылган сөйкөлөргө чейин, бир жолуже эритмелерге же эриген туздарга, демек, бул көрүнүшкө туш болот. Электрдик диссоциацияны илимдин бүтүндөй бир тармагы - электрохимия изилдейт деп бекеринен айтылган эмес.
Эригенде эриткич суюктуктун молекулалары эриген заттын молекулалары менен химиялык байланышка кирип, солваттарды пайда кылат. Суудагы эритмеде туздар, кислоталар жана негиздер диссоциацияланууга эң жакын. Бул процесстин натыйжасында эриген заттын молекулалары иондорго ажырай алат. Мисалы, суудагы эриткичтин таасири астында NaCl иондук кристаллдагы Na+ жана CI- иондору эриткич чөйрөгө өтүшөт. эритилген (гидратталган) бөлүкчөлөрдүн жаңы сапаты.
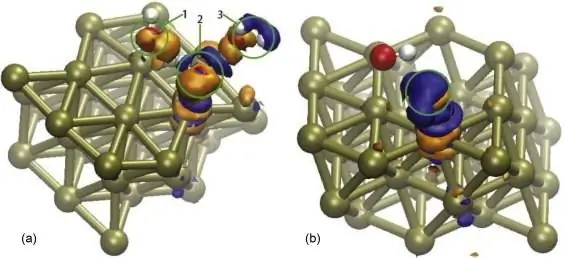
Негизинен эриген заттын иондорго толук же жарым-жартылай ажыроо процесси эриткичтин аракетинин натыйжасында «электрдик диссоциация» деп аталат. Бул процесс электрохимия үчүн өтө маанилүү. Татаал көп компоненттүү системалардын диссоциацияланышы этаптуу агым менен мүнөздөлүшү чоң мааниге ээ. Бул кубулуш менен эритмедеги иондордун саны да кескин көбөйөт, бул электролиттик заттарды электролиттик эмес заттардан айырмалайт.
Электролиз процессинде иондордун кыймылынын так багыты бар: оң заряддуу бөлүкчөлөр (катиондор) - катод деп аталган терс заряддуу электродго, ал эми оң иондор (аниондор) - анодго, бир карама-каршы заряддуу электрод, алар разряддалат. Катиондор калыбына келтирилип, аниондор кычкылданат. Демек, диссоциация кайра жаралуучу процесс.
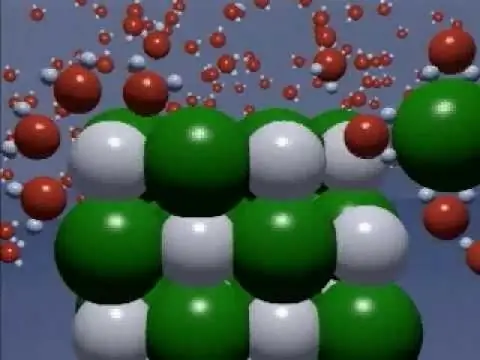
Бул электрохимиялык процесстин негизги мүнөздөмөлөрүнүн бири гидратталган бөлүкчөлөрдүн санынын эриген заттын молекулаларынын жалпы санына катышы катары туюнтулган электролиттик диссоциациянын даражасы. Бул көрсөткүч канчалык жогору болсо, электролит бул зат ошончолук күчтүү болот. Мунун негизинде бардык заттар алсыз, орточо күчтүү жана күчтүү электролиттер болуп бөлүнөт.
Диссоциациялануу даражасы төмөнкү факторлорго көз каранды: а) эриген заттын табиятына; б) эриткичтин табияты, анын диэлектрдик өтүмдүүлүгү жана полярдуулугу; в) эритменин концентрациясы (бул көрсөткүч канчалык төмөн болсо, диссоциациялануу даражасы ошончолук чоң болот); г) эрүүчү чөйрөнүн температурасы. Мисалы, уксус кислотасынын диссоциациясын төмөнкү формула менен туюндуруп алууга болот:
CH3COOH H+ + CH3COO-
Күчтүү электролиттер дээрлик кайтарылгыс диссоциацияланат, анткени алардын суудагы эритмесинде баштапкы молекулалар жана гидратланбаган иондор жок. Ошондой эле химиялык байланыштардын иондук жана коваленттик полярдуу түрүнө ээ болгон бардык заттар диссоциация процессине дуушар болоорун кошумчалоо керек. Электролиттик диссоциация теориясын 1887-жылы швед физиги жана химиги Сванте Аррениус чыгарган.
Сунушталууда:
Электрдик кран-балканын иштөө принциби

Электр устундуу кран - оор жүктөрдү ташуу үчүн цехтин имаратында шыптын астына орнотулган түзүлүш. Нур кран өзү бир кыйла жөнөкөй түзүлүш болуп саналат. Анын иштөө принциби жана түзүлүшү төмөндө талдоого алынат
Электрдик балка: моделдерге сереп салуу

Бүгүнкү күндө адистердин жардамысыз эле үйдө оңдоо иштерин өз алдынча жүргүзүүгө болот. рынокто сунушталган курал коопсуз жана кыйынчылыксыз да татаал орнотуу иштерин жүргүзүүгө мүмкүндүк берет. Бул электр балкасынын өзгөчөлүктөрү менен тастыкталат, анын аркасында көптөгөн адамдар кайра иштеп чыгууну жасашат. Бул ылайыктуу моделди чечүү үчүн гана калат
Электрдик болот: өндүрүү жана колдонуу

Болаттын бул түрүн өндүрүү башка магниттик материалдардын арасында алдыңкы орунду ээлейт. Электрдик болот - темирдин кремний менен эритмеси, анын үлүшү 0,5%тен 5%ке чейин
Айдоочунун ишмердүүлүгүнүн психофизиологиялык негиздери. Айдоочунун эмгегинин психофизиологиясынын негиздери

Айдоо курсуна келгенде, ар бир адам жолдо жүрүм-турум эрежелерин үйрөнүү менен бирге, айдоочунун иш-аракетинин психофизиологиялык негиздерин изилдөөгө туура келерине даяр эмес. Бирок бул суроолор машинага ээ болуу чеберчилигинен кем эмес маанилүү
Финансылык-чарбалык иштин анализи – теориялык негиздери

Рынок мамилелерине өтүү бардык ишканалардан өндүрүштүн эффективдүүлүгүн жогорулатууну талап кылат, бул болсо өз кезегинде продукциянын атаандаштыкка жөндөмдүүлүгүн жогорулатат. Бул проблеманы чечууде финансы-чарбалык ишти талдоо эц маанилуу роль ойнойт. Бул илимий дисциплинанын жардамы менен өнүгүүнүн стратегиялык пландары түзүлүп, башкаруу чечимдери илимий жактан негизделип, алардын аткарылышы көзөмөлдөнөт

